未治療進行EGFR遺伝子変異陽性肺癌に対する新たな初回治療 [EGFR遺伝子変異陽性肺癌]
 今年に入ってからEGFR遺伝子変異陽性肺癌に対する新たなエビデンスが続々登場しています。今後、オシメルチニブ(タグリッソ)が初回治療での追加承認がなされれば、副作用が少なく効果がより高い治療薬が患者さんに届けることができるようになります。今日はそのエビデンスの紹介です。
ただ、このオシメルチニブ単剤の治療の他、化学療法+ゲフィチニブ(イレッサ)、血管新生阻害薬(ベバシズマブ)+エルロチニブ(タルセバ)の有効性のエビデンスも今年のASCOで発表されており、治療の選択肢が広がっています。
今年に入ってからEGFR遺伝子変異陽性肺癌に対する新たなエビデンスが続々登場しています。今後、オシメルチニブ(タグリッソ)が初回治療での追加承認がなされれば、副作用が少なく効果がより高い治療薬が患者さんに届けることができるようになります。今日はそのエビデンスの紹介です。
ただ、このオシメルチニブ単剤の治療の他、化学療法+ゲフィチニブ(イレッサ)、血管新生阻害薬(ベバシズマブ)+エルロチニブ(タルセバ)の有効性のエビデンスも今年のASCOで発表されており、治療の選択肢が広がっています。
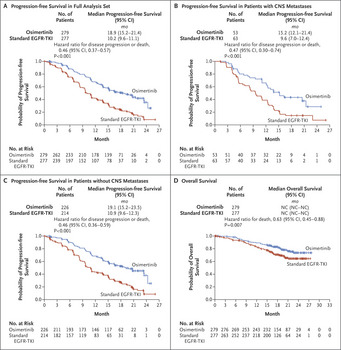
Osimertinib in Untreated EGFR-Mutated Advanced Non–Small-Cell Lung Cancer N Engl J Med 2018; 378:113-125 未治療進行EGFR遺伝子変異陽性肺癌に対するオシメルチニブとゲフィチニブまたはエルロチニブを比較した第三相試験(FLAURA試験) EGFR遺伝子変異陽性肺癌に対する初回治療薬として、現在日本ではゲフィチニブ、エルロチニブ、アファチニブの3剤が保険承認されています。通常はこれらの3剤のいずれかを初回治療のEGFR-TKIとして選択するのですが、第二世代であるアファチニブを除いたゲフィチニブとエルロチニブの2剤とオシメルチニブの有用性を直接比較した第三相試験がこのFLAURA試験です。 結果は、主要評価項目である無増悪生存期間がオシメルチニブ群18.9ヶ月、コントロール群10.2ヶ月と半年以上の差をつけてオシメルチニブが優れている結果でした(ハザード比0.46、95%信頼区間0.37-0.57、P<0.001)。グレード3以上の有害事象の頻度もオシメルチニブ群で有意に少なかった(34% vs 45%)からオシメルチニブの完全勝利の結果となった試験です。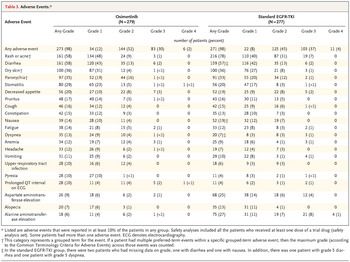 この結果をもとに、欧米では初回治療としてオシメルチニブが既に承認を受けていることから、日本でも現在、適応拡大の申請がなされており、近い将来、初回治療としてオシメルチニブが使えるようになると思われます。 副作用が(少)なく、抗腫瘍効果が高い。これが治療薬の理想であり、日本で開発されたALK阻害剤であるアレクチニブ(アレセンサ)がその代表と言えます。オシメルチニブも同様の薬に近いので、今後、オシメルチニブの活躍の場が広がっていくのではないかと思われます。 一方で、オシメルチニブにも耐性の問題がありますので、その耐性機序の解明と克服が今後も課題として残ります。
この結果をもとに、欧米では初回治療としてオシメルチニブが既に承認を受けていることから、日本でも現在、適応拡大の申請がなされており、近い将来、初回治療としてオシメルチニブが使えるようになると思われます。 副作用が(少)なく、抗腫瘍効果が高い。これが治療薬の理想であり、日本で開発されたALK阻害剤であるアレクチニブ(アレセンサ)がその代表と言えます。オシメルチニブも同様の薬に近いので、今後、オシメルチニブの活躍の場が広がっていくのではないかと思われます。 一方で、オシメルチニブにも耐性の問題がありますので、その耐性機序の解明と克服が今後も課題として残ります。
未治療EGFR陽性肺がんに対するオシメルチニブ(タグリッソ)の有効性 [EGFR遺伝子変異陽性肺癌]
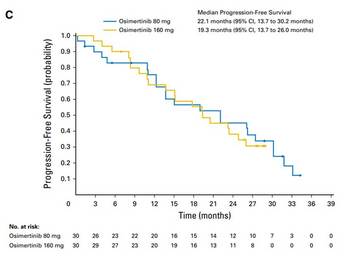
2018年3月号のJCOに未治療EGFR遺伝子変異陽性肺がん患者に対する初回治療としてのオシメルチニブの有効性データが掲載されました。無増悪生存期間中央値は22.1ヶ月で2年に迫る結果です。 日本人では初回治療として第二世代のEGFR-TKIであるアファチニブ(ジオトリフ)を投与した場合、無増悪生存期間中央値は13-16ヶ月であることからさらに半年以上の有効性が期待できる結果となっています。 ただ、現状では、第一世代(ゲフィチニブ、エルロチニブ)または第二世代(アファチニブ)増悪後にT790M耐性変異が認められた場合(約50%の患者さんでみつかります)には二次治療としてオシメルチニブが投与されています。 そこで、 ①初回からオシメルチニブ ②ゲフィチニブ、エルロチニブ、アファチニブのいずれかを使用後、T790M変異を確認してオシメルチニブ のどちらの治療戦略が患者さんにとって有益かとの議論になります。 データを見る限りでは、効果と安全性のバランスから、初回からオシメルチニブを使う方が将来的に増えることが予想されます。
Osimertinib As First-Line Treatment of EGFR Mutation–Positive Advanced Non–Small-Cell Lung Cancer
J Clin Oncol. 2018 Mar 20;36(9):841-849. doi: 10.1200/JCO.2017.74.7576
Abstract
Purpose The AURA study ( ClinicalTrials.gov identifier: NCT01802632) included two cohorts of treatment-naïve patients to examine clinical activity and safety of osimertinib (an epidermal growth factor receptor [EGFR] -tyrosine kinase inhibitor selective for EGFR-tyrosine kinase inhibitor sensitizing [ EGFRm] and EGFR T790M resistance mutations) as first-line treatment of EGFR-mutated advanced non-small-cell lung cancer (NSCLC).
Patients and Methods
Sixty treatment-naïve patients with locally advanced or metastatic EGFRm NSCLC received osimertinib 80 or 160 mg once daily (30 patients per cohort). End points included investigator-assessed objective response rate (ORR), progression-free survival (PFS), and safety evaluation. Plasma samples were collected at or after patients experienced disease progression, as defined by Response Evaluation Criteria in Solid Tumors (RECIST), to investigate osimertinib resistance mechanisms.
Results
At data cutoff (November 1, 2016), median follow-up was 19.1 months. Overall ORR was 67% (95% CI, 47% to 83%) in the 80-mg group, 87% (95% CI, 69% to 96%) in the 160-mg group, and 77% (95% CI, 64% to 87%) across doses. Median PFS time was 22.1 months (95% CI, 13.7 to 30.2 months) in the 80-mg group, 19.3 months (95% CI, 13.7 to 26.0 months) in the 160-mg group, and 20.5 months (95% CI, 15.0 to 26.1 months) across doses. Of 38 patients with postprogression plasma samples, 50% had no detectable circulating tumor DNA. Nine of 19 patients had putative resistance mechanisms, including amplification of MET (n = 1); amplification of EGFR and KRAS (n = 1); MEK1, KRAS, or PIK3CA mutation (n = 1 each); EGFR C797S mutation (n = 2); JAK2 mutation (n = 1); and HER2 exon 20 insertion (n = 1). Acquired EGFR T790M was not detected.
Conclusion
Osimertinib demonstrated a robust ORR and prolonged PFS in treatment-naïve patients with EGFRm advanced NSCLC. There was no evidence of acquired EGFR T790M mutation in postprogression plasma samples.
タルセバとアバスチンの併用療法(JO25567試験) [EGFR遺伝子変異陽性肺癌]
2014年8月のLancet OncologyにJO25567試験が掲載されました。
この試験は、EGFR遺伝子変異陽性の非小細胞肺がんの一次治療におけるエルロチニブ(商品名:タルセバ)とベバシズマブ(商品名:アバスチン)の併用療法とエルロチニブの単剤療法の有効性および安全性について比較検討することを目的として行われた第二相ランダム化試験です。
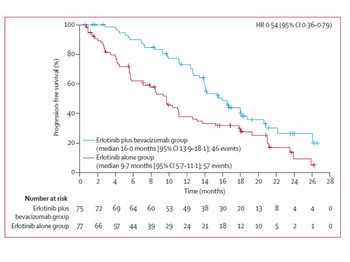
当初、この試験はそれほど注目されていませんでした。タルセバにアバスチンを上乗せしたくらいでそんなに効果に差が出るだろうと思っていない人が多かったからです。
しかし、上記のように、タルセバにアバスチンを上乗せすることにより6か月もの無増悪生存期間の延長が示されました。
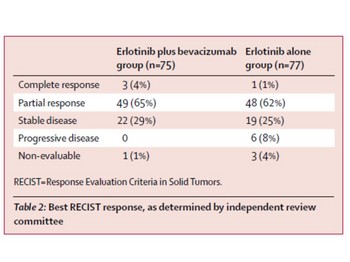
奏効率は上記のように大差ありません。
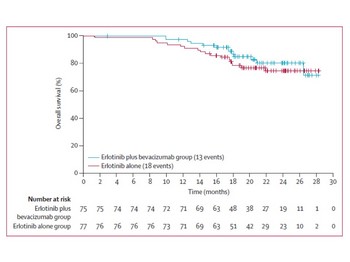
OSの解析は行われていませんが、曲線をみる限りは差が出そうな勢いです。
この結果を単純にみてしまうと、タルセバ+アバスチンは標準治療として日常診療に受け入れられそうですが、あくまでこの試験は第二相ランダム化試験ですので、エビデンスレベルは低いと判断します。つまり、この試験1本の結果でタルセバ+アバスチン療法は素晴らしいという結論は時期尚早だと言えます。
実は、欧米でも同様の試験が行われており、当初はその試験の結果も合わせて結論を出す予定でしたが、症例集積が進まないこともあり最終的な結論には時間がかかりそうなため、日本で上記試験の検証が行われそうです。
最終的な結論は今後行われる上記を検証する第三相試験の結果待ちとなりそうです。
この試験は、EGFR遺伝子変異陽性の非小細胞肺がんの一次治療におけるエルロチニブ(商品名:タルセバ)とベバシズマブ(商品名:アバスチン)の併用療法とエルロチニブの単剤療法の有効性および安全性について比較検討することを目的として行われた第二相ランダム化試験です。
当初、この試験はそれほど注目されていませんでした。タルセバにアバスチンを上乗せしたくらいでそんなに効果に差が出るだろうと思っていない人が多かったからです。
しかし、上記のように、タルセバにアバスチンを上乗せすることにより6か月もの無増悪生存期間の延長が示されました。
奏効率は上記のように大差ありません。
OSの解析は行われていませんが、曲線をみる限りは差が出そうな勢いです。
この結果を単純にみてしまうと、タルセバ+アバスチンは標準治療として日常診療に受け入れられそうですが、あくまでこの試験は第二相ランダム化試験ですので、エビデンスレベルは低いと判断します。つまり、この試験1本の結果でタルセバ+アバスチン療法は素晴らしいという結論は時期尚早だと言えます。
実は、欧米でも同様の試験が行われており、当初はその試験の結果も合わせて結論を出す予定でしたが、症例集積が進まないこともあり最終的な結論には時間がかかりそうなため、日本で上記試験の検証が行われそうです。
最終的な結論は今後行われる上記を検証する第三相試験の結果待ちとなりそうです。



