未治療EGFR陽性肺がんに対するオシメルチニブ(タグリッソ)の有効性 [EGFR遺伝子変異陽性肺癌]
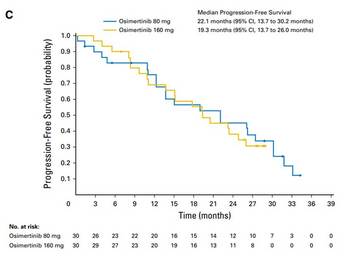
2018年3月号のJCOに未治療EGFR遺伝子変異陽性肺がん患者に対する初回治療としてのオシメルチニブの有効性データが掲載されました。無増悪生存期間中央値は22.1ヶ月で2年に迫る結果です。 日本人では初回治療として第二世代のEGFR-TKIであるアファチニブ(ジオトリフ)を投与した場合、無増悪生存期間中央値は13-16ヶ月であることからさらに半年以上の有効性が期待できる結果となっています。 ただ、現状では、第一世代(ゲフィチニブ、エルロチニブ)または第二世代(アファチニブ)増悪後にT790M耐性変異が認められた場合(約50%の患者さんでみつかります)には二次治療としてオシメルチニブが投与されています。 そこで、 ①初回からオシメルチニブ ②ゲフィチニブ、エルロチニブ、アファチニブのいずれかを使用後、T790M変異を確認してオシメルチニブ のどちらの治療戦略が患者さんにとって有益かとの議論になります。 データを見る限りでは、効果と安全性のバランスから、初回からオシメルチニブを使う方が将来的に増えることが予想されます。
Osimertinib As First-Line Treatment of EGFR Mutation–Positive Advanced Non–Small-Cell Lung Cancer
J Clin Oncol. 2018 Mar 20;36(9):841-849. doi: 10.1200/JCO.2017.74.7576
Abstract
Purpose The AURA study ( ClinicalTrials.gov identifier: NCT01802632) included two cohorts of treatment-naïve patients to examine clinical activity and safety of osimertinib (an epidermal growth factor receptor [EGFR] -tyrosine kinase inhibitor selective for EGFR-tyrosine kinase inhibitor sensitizing [ EGFRm] and EGFR T790M resistance mutations) as first-line treatment of EGFR-mutated advanced non-small-cell lung cancer (NSCLC).
Patients and Methods
Sixty treatment-naïve patients with locally advanced or metastatic EGFRm NSCLC received osimertinib 80 or 160 mg once daily (30 patients per cohort). End points included investigator-assessed objective response rate (ORR), progression-free survival (PFS), and safety evaluation. Plasma samples were collected at or after patients experienced disease progression, as defined by Response Evaluation Criteria in Solid Tumors (RECIST), to investigate osimertinib resistance mechanisms.
Results
At data cutoff (November 1, 2016), median follow-up was 19.1 months. Overall ORR was 67% (95% CI, 47% to 83%) in the 80-mg group, 87% (95% CI, 69% to 96%) in the 160-mg group, and 77% (95% CI, 64% to 87%) across doses. Median PFS time was 22.1 months (95% CI, 13.7 to 30.2 months) in the 80-mg group, 19.3 months (95% CI, 13.7 to 26.0 months) in the 160-mg group, and 20.5 months (95% CI, 15.0 to 26.1 months) across doses. Of 38 patients with postprogression plasma samples, 50% had no detectable circulating tumor DNA. Nine of 19 patients had putative resistance mechanisms, including amplification of MET (n = 1); amplification of EGFR and KRAS (n = 1); MEK1, KRAS, or PIK3CA mutation (n = 1 each); EGFR C797S mutation (n = 2); JAK2 mutation (n = 1); and HER2 exon 20 insertion (n = 1). Acquired EGFR T790M was not detected.
Conclusion
Osimertinib demonstrated a robust ORR and prolonged PFS in treatment-naïve patients with EGFRm advanced NSCLC. There was no evidence of acquired EGFR T790M mutation in postprogression plasma samples.
2018-04-12 03:58
nice!(1)
コメント(0)




コメント 0